Indikationer
Behandling och prevention av tecken och symtom på säsongsbunden och perenn allergisk rinit.
Behandling av tecken och symtom på näspolyper.
Kontraindikationer
Överkänslighet mot den aktiva substansen eller mot något hjälpämne som anges i avsnitt Innehåll.
Dosering
Endast avsett för nasal användning.
Doseringen ska bestämmas individuellt. Dosen ska titreras till lägsta dos vid vilken effektiv kontroll av symtomen bibehålls.
Längden på behandlingen med Desonix bör begränsas till perioden av allergenexponeringen och beror på allergenets natur och karaktäristik. För full behandlingseffekt krävs regelbunden användning.
Allergisk rinit
Startdos
Vuxna, ungdomar och barn från 6 års ålder:
Den rekommenderade startdosen på 256 mikrogram kan administreras en gång dagligen på morgonen eller delas upp på två dostillfällen, morgon och kväll.
Desonix 32 mikrogram/dos nässpray, suspension
4 sprayningar i varje näsborre en gång dagligen på morgonen eller
2 sprayningar i varje näsborre morgon och kväll.
Desonix 64 mikrogram/dos nässpray, suspension
2 sprayningar i varje näsborre en gång dagligen på morgonen eller
1 sprayning i varje näsborre morgon och kväll.
Barn ska behandlas under vägledning av en vuxen
Behandling av säsongsbunden allergisk rinit ska om möjligt sättas in innan patienten exponeras för allergener.
Samtidig behandling kan ibland krävas för behandling av allergisymtom som påverkar ögonen.
Underhållsdos
Önskad klinisk effekt uppnås inom cirka 1-2 veckor.
Därefter ska lägsta möjliga effektiva dos väljas som håller patienten symtomfri.
Ingen ytterligare effekt kan förväntas vid högre doser än 256 mikrogram.
Näspolyper
Vuxna, ungdomar och barn från 6 års ålder:
Rekommenderad dos för behandling av näspolyper är 256 mikrogram. Dosen kan administreras en gång dagligen på morgonen eller delas upp på två dostillfällen, morgon och kväll.
Desonix 32 mikrogram/dos nässpray, suspension
4 sprayningar i varje näsborre en gång dagligen på morgonen eller
2 sprayningar i varje näsborre morgon och kväll.
Desonix 64 mikrogram/dos nässpray, suspension
2 sprayningar i varje näsborre en gång dagligen på morgonen eller
1 sprayning i varje näsborre morgon och kväll.
Barn ska behandlas under vägledning av en vuxen.
Efter att önskad klinisk effekt har uppnåtts ska man välja lägsta möjliga effektiva dos som håller patienten symtomfri.
Administreringssätt
1. Vid behov, snyt dig försiktigt så att näsan blir ren.
2. Skaka flaskan (figur 1). Ta bort skyddslocket.
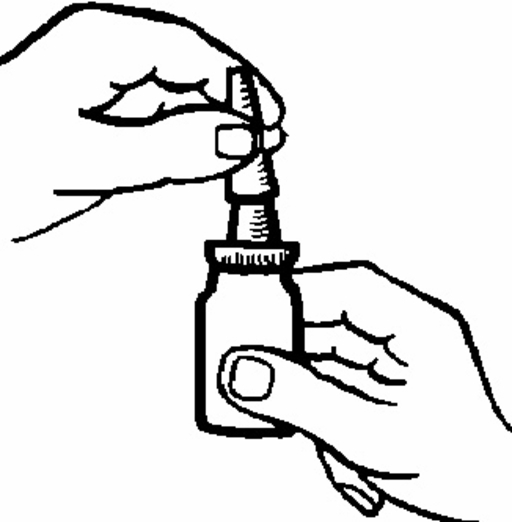
Figur 1.
3. Håll flaskan enligt figur 2. Innan du använder Desonix första gången måste du ladda näsapplikatorn (dvs. fylla den med läkemedel). Pumpa näsapplikatorn upp och ned flera gånger (5-10 gånger), spraya i luften till du får en jämn dusch. Laddningseffekten kvarstår ungefär ett dygn. Om det går längre tid innan nästa dos tas måste näsapplikatorn laddas (fyllas med läkemedel) igen. Om Desonix används med kortare mellanrum räcker det att bara spraya en gång i luften.
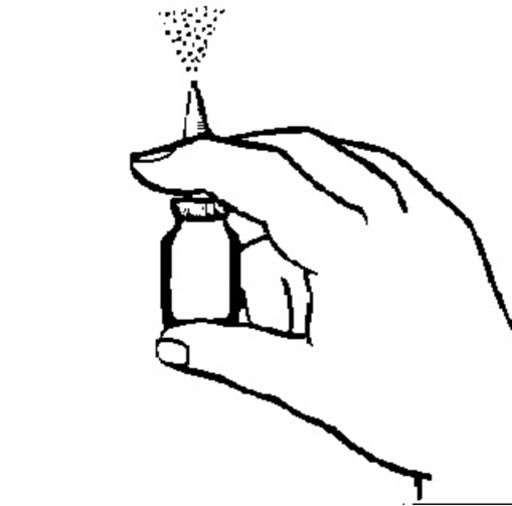
Figur 2.
4. För in spetsen på näsapplikatorn i näsborren enligt figur 3 och spraya en gång (eller mer om din läkare har ordinerat detta). Använd sprayen i den andra näsborren på samma sätt. Tänk på att du inte behöver andas in samtidigt som du sprayar.
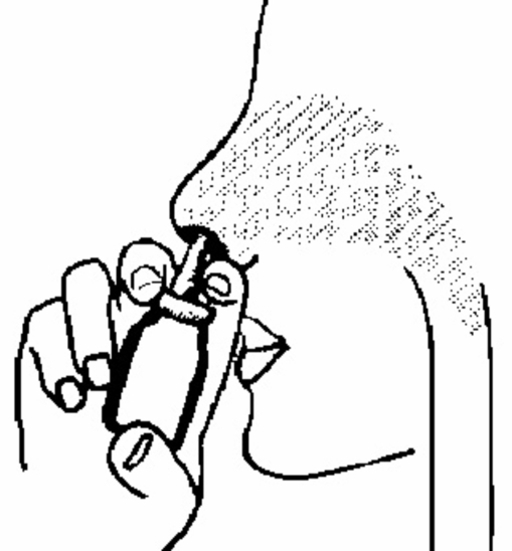
Figur 3.
5. Torka av spetsen på näsapplikatorn med ett rent hushållspapper och sätt på skyddslocket igen.
6. Förvara flaskan i upprätt läge.
Rengöring av din Desonix
Du bör rengöra näsapplikatorns plastspets på Desonix regelbundet och alltid när sprayen med läkemedlet inte kommer ut som det ska. Om detta händer ska du först kontrollera att näsapplikatorn är laddad med läkemedel (se tidigare beskrivning). Om näsapplikatorns pump fortfarande inte fungerar efter att du har laddat den igen ska du rengöra näsapplikatorn enligt följande:
-
Ta bort näsapplikatorn med ett rent hushållspapper och skölj av den i varmt – inte hett – vatten.
-
Skölj näsapplikatorn noggrant, torka den och sätt sedan tillbaka den på flaskans övre del.
-
Försök aldrig att rengöra näsapplikatorn genom att använda en nål eller något annat spetsigt föremål.
Efter rengöring av näsapplikatorn måste den laddas igen (fyllas med läkemedel) innan den kan användas.
Varningar och försiktighet
Systemeffekter av nasala kortikosteroider kan uppträda, särskilt vid höga doser, när de ordinerats under långa perioder tillsammans med tilläggsbehandling eller tidigare behandling med kortikoider, samt beroende på individuella faktorer. Det är mindre troligt att denna påverkan uppträder vid intranasal behandling jämfört med när kortikosteroider ges peroralt och denna påverkan kan variera mellan patienter och för olika kortikosteroidpreparat. Eventuella systembiverkningar kan inkludera Cushings syndrom, Cushingliknande symtombild, binjuresuppression, hämmad längdtillväxt hos barn och ungdomar, katarakt, glaukom, och mer sällsynt en rad psykologiska störningar eller beteendestörningar innefattande psykomotorisk hyperaktivitet, sömnstörningar, oro, depression eller aggression (särskilt hos barn).
Behandling med högre doser nasala kortikosteroider än de rekommenderade kan medföra kliniskt signifikant binjuresuppression. Om det finns belägg för högre doser än de rekommenderade ska man överväga ytterligare skydd med systemiska kortikosteroider under en period av stress eller inför planerad operation.
Vid infektioner i näsan orsakade av bakterier eller svamp ska Desonix endast användas om samtidig antibakteriell behandling eller behandling mot svamp genomförs.
Vid kontinuerlig långtidsbehandling ska näsans slemhinna inspekteras regelbundet, t.ex. var sjätte månad.
Nedsatt leverfunktion påverkar farmakokinetiken av kortikosteroider. Grav nedsättning av leverfunktionen påverkar farmakokinetiken, inklusive elimineringen, av oralt administrerat budesonid, vilket medför ökad systemisk tillgänglighet och minskad elimineringskapacitet. Farmakokinetiken av intravenöst administrerat budesonid hos friska frivilliga och patienter med levercirros är emellertid ungefär likartad. Hänsyn kan behöva tas till eventuellt uppkommande systemeffekter vid grav nedsättning av leverfunktionen. Detta har dock begränsad klinisk relevans för budesonid nässpray, eftersom endast en relativt liten mängd oralt innehåll är systemiskt tillgänglig efter nasal administrering.
Desonix bör inte användas av patienter med epistaxis eller herpesinfektion i mun-, näs- eller ögonregion.
Desonix rekommenderas inte till patienter med sår i näsan, vid nyligen genomgången operation eller nasalt trauma, förrän fullständig återhämtning skett.
Särskild försiktighet måste iakttas vid behandling av patienter med aktiv eller latent lungtuberkulos samt patienter med svamp- eller virusinfektioner i luftvägarna.
Patienten ska informeras om att full effekt inte uppnås förrän efter några dagars behandling. Behandling av säsongsbunden rinit bör om möjligt påbörjas före exponeringen för allergener.
Synrubbning
Synrubbning kan rapporteras vid systemisk och topisk användning av kortikosteroider. Om en patient inkommer med symtom såsom dimsyn eller andra synrubbningar bör man överväga att remittera patienten till en oftalmolog för utredning av möjliga orsaker. Dessa kan innefatta katarakt, glaukom eller sällsynta sjukdomar såsom central serös korioretinopati (CSCR), som har rapporterats efter användning av systemiska och topiska kortikosteroider.
Detta läkemedel innehåller kaliumsorbat och kan ge hudirritationer (t.ex. kontaktdermatit).
Pediatrisk population
Långtidseffekterna då barn behandlas med nasala glukokortikosteroider är inte helt kända. Läkaren bör noggrant följa tillväxten hos barn som tar glukokortikosteroider en längre tid, oavsett administreringssätt, och väga fördelarna med glukokortikosteroidbehandlingen mot risken för tillväxthämning.
Tillväxthämning har rapporterats hos barn som får nasala kortikosteroider i godkända doser. Barn som behandlas längre tid med nasala kortiksteroider bör regelbundet kontrolleras avseende längdtillväxten. Om tillväxten avtar ska ny bedömning av behandlingen göras för att om möjligt sänka dosen av den nasala kortikosteroiden till den lägsta dos som fortfarande ger effektiv symtomkontroll. Även remiss till pedatrisk specialist bör övervägas.
Byte från systemisk till nasal administrering
Försiktighet måste iakttas när patienter byter från behandling med systemisk steroid till Desonix spray om det finns skäl att anta att binjurefunktionen är nedsatt.
Interaktioner
Inga interaktioner har iakttagits mellan budesonid och andra läkemedel som används för behandling av rinit.
Metabolismen av budesonid medieras främst via CYP3A4, en undergrupp av cytokrom P450. Hämmare av detta enzym, t.ex. ketokonazol, itrakonazol, ciklosporin, etinylestradiol och troleandomycin kan därför öka den systemiska exponeringen för budesonid flerfaldigt. Eftersom det inte finns några data som stödjer en dosrekommendation ska kombinationen undvikas. Om detta inte är möjligt ska tiden mellan administreringarna vara så lång som möjligt. En minskning av budesoniddosen kan också övervägas. När det gäller korttidsbehandling har detta begränsad klinisk signifikans.
Samtidig administrering av cimetidin och budesonid kan resultera i en liten ökning av plasmakoncentrationen av budesonid, vilket dock saknar klinisk signifikans.
Ökade plasmakoncentrationer och starkare effekt av kortikosteroider har observerats hos kvinnor som även behandlas med östrogener och kontraceptiva steroider, men ingen effekt har observerats då budesonid används samtidigt som kombinations-p-piller med låg dos.
Samtidig behandling med CYP3A-hämmare, inklusive läkemedel som innehåller kobicistat, väntas öka risken för systemiska biverkningar. Kombinationen ska undvikas såvida inte nyttan uppväger den ökade risken för systemiska biverkningar av kortikosteroider, och om så är fallet ska patienter övervakas avseende systemiska biverkningar av kortikosteroider.
Eftersom binjurefunktionen kan hämmas kan ett ACTH-test för diagnostik av hypofysinsufficiens visa felaktiga resultat (för låga värden).
Graviditet
Resultat från prospektiva epidemiologiska studier och globala erfarenheter efter försäljningsstarten tyder inte på att inhalerat eller intranasalt budesonid under tidig graviditet medför ökad risk för medfödda missbildningar. Djurstudier har visat reproduktionstoxikologiska effekter (se avsnitt Prekliniska uppgifter). Betydelsen av dessa för människa är okänd. Liksom för andra läkemedel gäller vid administrering av budesonid att fördelarna för modern måste vägas mot riskerna för fostret. Användningen av budesonid ska vara så kortvarig som möjligt.
Amning
Budesonid utsöndras i bröstmjölk men vid terapeutiska doser av budesonid förväntas inga effekter på spädbarn som ammas. Budesonid kan användas under amning.
Underhållsbehandling med inhalerat budesonid (200 eller 400 mikrogram två gånger dagligen) till ammande kvinnor med astma resulterar i obetydlig systemisk exponering för budesonid hos spädbarnen som ammas.
I en farmakokinetisk studie beräknades den dagliga dosen för spädbarnet till 0,3 % av den dagliga dosen för modern vid båda dosnivåerna. Den genomsnittliga plasmakoncentrationen hos spädbarnet beräknades till 1/600-del av plasmakoncentrationen hos modern, under antagande av fullständig oral biotillgänglighet hos barnet. Budesonidkoncentrationen i plasmaprover från spädbarn låg i samtliga prover under gränsen för mätbart värde.
Baserat på data från inhalerat budesonid och att budesonid uppvisar linjära PK-egenskaper inom det terapeutiska dosintervallet efter nasal, inhalerad, oral och rektal administrering av läkemedlet i terapeutiska doser, förväntas exponeringen hos det ammade barnet vara låg.
Trafik
Desonix har ingen effekt på förmågan att framföra fordon och använda maskiner.
Biverkningar
När patienter överförs från en systemisk kortikosteroid (oral eller parenteral) till Desonix kan oönskade effekter utanför näsområdet uppstå, vilka tidigare var under kontroll genom den systemiska behandlingen, t.ex. allergisk konjunktivit eller dermatit. Tilläggsbehandling av dessa effekter bör ske vid behov.
I sällsynta fall kan nasala glukokortikosteroidberedningar ge fynd eller symtom på systemiska glukokortikosteroidbiverkningar, vilket förmodligen beror på den använda dosen, exponeringstiden, samtidig eller tidigare kortikosteroidexponering samt individuell känslighet.
Biverkningarna presenteras inom varje frekvensområde efter fallande allvarlighetsgrad.
Mycket vanliga: (≥1/10)
Vanliga: (≥1/100, <1/10)
Mindre vanliga: (≥1/1 000, <1/100)
Sällsynta: (≥1/10 000, <1/1 000)
Mycket sällsynta: (<1/10 000)
Ingen känd frekvens (kan inte beräknas från tillgängliga data)
|
Organsystem |
Frekvens |
Biverkning |
|
Immunsystemet |
Mindre vanliga |
Omedelbar eller fördröjd överkänslighetsreaktion (urtikaria, utslag, klåda, dermatit, angioödem) |
|
|
Sällsynta |
Anafylaktisk reaktion |
|
Endokrina systemet |
Sällsynta |
Tecken och symtom på systemiska kortikosteroideffekter, såsom binjuresuppression och tillväxt-hämning hos barn (se avsnitt Varningar och försiktighet) |
|
|
|
|
|
Ögon |
Sällsynta |
Glaukom, katarakt (vid långtids-behandling), dimsyn (se även avsnitt Varningar och försiktighet) |
|
Andningsvägar, bröstkorg och mediastinum |
Vanliga |
Lokala symptom som irritation i näsans slemhinna, lätt hemorragisk nässekretion, epistaxis (omedelbart efter appliceringen) |
|
|
Sällsynta |
Sår i näsan, nässeptumperforation, dysfoni |
|
Hud och subkutan vävnad |
Sällsynta |
Blåmärken |
|
Muskuloskeletala systemet och bindväv |
Mindre vanliga |
Muskelspasm |
|
|
Sällsynta |
Osteoporos (vid långtids-behandling) |
Pediatrisk population
Tillväxthämning har rapporterats hos barn som får intranasala steroider. På grund av risken för tillväxthämning i den pediatriska populationen ska tillväxten övervakas enligt beskrivning i avsnitt Varningar och försiktighet.
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar efter att läkemedlet godkänts. Det gör det möjligt att kontinuerligt övervaka läkemedlets nytta-riskförhållande. Hälso- och sjukvårdspersonal uppmanas att rapportera varje misstänkt biverkning till Läkemedelsverket, men alla kan rapportera misstänkta biverkningar till Läkemedelsverket, www.lakemedelsverket.se. Postadress
Läkemedelsverket
Box 26
751 03 Uppsala
Överdosering
Akut överdosering med Desonix är osannolik även om allt innehåll i en flaska skulle tillföras genom sprayning vid ett tillfälle. Akut överdosering med budesonid förväntas inte vara kliniskt relevant. Administrering av högre doser än de rekommenderade (se avsnitt Dosering och administrationssätt) under en lång period (under månader) kan ge biverkningar.
Farmakodynamik
Budesonid är en glukokortikosteroid med kraftig lokal antiinflammatorisk effekt på näsans slemhinna och svaga systemeffekter efter lokal administrering.
Kortikosteroider har visats ha en bred hämmande verkan mot flera olika celltyper (t.ex. mastceller, eosinofiler, neutrofiler, makrofager och lymfocyter) och mediatorer (t.ex. histamin, eikosanoider, leukotriener och cytokiner) som är involverade i allergiskt medierade inflammationer. De reducerar även mängden cytokiner, leukotriener och kemokiner (t.ex. Il-1 till Il-6, RANTES, TNF-α, IFN -γ och GM-CSF) som utsöndras av inflammatoriska celler. Budesonid binder till glukokortikoidreceptorer och bildar ett komplex som fungerar som en transkriptionsfaktor genom att antingen nedreglera proinflammatoriska mediatorer eller uppreglera antiinflammatoriska mediatorer. Man antar att det finns omkring 10–100 steroidresponsiva gener per cell.
Pediatrisk population
Klinisk effekt
Den terapeutiska effekten av budesonid nässpray har utvärderats på flera tusen vuxna och barn. De flesta studier genomfördes med intranasalt tillförda doser på mellan 32 och 256 µg budesonid en gång dagligen. Exempel på representativa studier som utvärderar användningen av budesonid för behandling av barn med säsongsbunden och perenn allergisk rinit finns nedan. Den primära effektvariabeln var kombinerade nässymtompoäng (CNSS, combined nasal symptoms score), som är summan av de individuella nässymtompoängen för tre nässymtom (nästäppa, rinnande näsa och nysningar, som var och en skattats enligt en skala på 0-3).
Säsongsbunden allergisk rinit
En 2 veckors randomiserad, dubbelblind placebokontrollerad studie med parallella grupper utvärderade effekt och säkerhet för budesonid nässpray 16, 32 och 64 µg en gång dagligen på 400 barn (i åldern 2 till 5 år) med allergisk rinit (säsongsbunden eller perenn). Det skedde en markant minskning från utgångsvärdet för CNSS i alla behandlingsgrupper, inklusive placebo. Skillnaden mellan budesonid nässpray 64 µg och placebobehandling var inte statistiskt signifikant.
Perenn allergisk rinit
En 6 veckors randomiserad, dubbelblind, placebokontrollerad studie med parallella grupper utvärderade effekt och säkerhet av budesonid nässpray 128 µg en gång dagligen på 202 barn (i åldern 6 till 16 år) med perenn allergisk rinit. Primära effektvariabler var CNSS och värden för maximalt nasalt inandningsflöde (PNIF, peak nasal inspiratory flow). Budesonid nässpray gav statistiskt signifikant större förbättring av CNSS och PNIF än placebo. Effekttillslaget för budesonid nässpray skedde 12 timmar efter den första dosen för CNSS och 48 timmar för PNIF.
Klinisk säkerhet
I en randomiserad, dubbelblind, placebokontrollerad tillväxstudie fick 229 prepubertala barn i åldern 4 till 8 år budesonid nässpray 64 mikrogram en gång dagligen eller placebo i 12 månader efter en 6 månaders baslinjeperiod. I den här studien var tillväxthastigheten likartad mellan grupperna som fick budesonid nässpray respektive placebo efter 12 månaders behandling. Den genomsnittliga skillnaden i tillväxthastighet (placebo budesonid nässpray) var 0,27 cm/år (95 % konfidensintervall: –0,07 till 0,62).
Påverkan på kortisolkoncentrationen i plasma:
Vid rekommenderade doser orsakar budesonid inte några kliniskt relevanta förändringar av basala kortisolkoncentrationer i plasma eller av ACTH-stimulering. Hos friska frivilliga sågs en dosberoende suppression av koncentrationerna av kortisol i plasma och urin efter kortvarig administrering av budesonid nässpray.
Farmakokinetik
Absorption
Nasal administrering av budesonid vid säsongsbunden och kronisk rinit leder inte enbart till absorption genom näsans slemhinna utan också till gastrointestinal absorption av den aktiva substansen, eftersom den sväljs ner till följd av ökad produktion av slem i näsan. Den svalda fraktionen leder till mycket låga plasmanivåer på grund av den höga första passage-effekten för budesonid.
Den systemiska tillgängligheten av budesonid från budesonid nässpray är 33 % av avgiven dos. Maximal plasmakoncentration hos vuxna efter administrering av 256 mikrogram budesonid från budesonid nässpray är 0,64 nmol/l, och nås inom 0,7 timmar. AUC (area under kurvan) efter administrering av 256 mikrogram budesonid från budesonid nässpray är 2,7 nmol × timmar/l hos vuxna.
Distribution
Budesonid har en distributionsvolym på cirka 3 l/kg. Plasmaproteinbindningen är i genomsnitt 85-90 %.
Metabolism
Budesonid genomgår en omfattande (cirka 90 %) första-passage-metabolism i levern till metaboliter med låg glukokortikosteroidaktivitet. Glukokortikosteroidaktiviteten för huvudmetaboliterna, 6-beta-hydroxibudesonid och 16-alfa-hydroxiprednisolon, är mindre än 1 % av den för budesonid. Metabolismen av budesonid medieras främst av CYP3A, en subfamilj av cytokrom P450. Budesonid genomgår inte lokal metabol inaktivering i näsan.
Eliminering
Metaboliterna utsöndras som de är eller i konjugerad form, främst via njurarna. Inget intakt budesonid har detekterats i urin. Budesonid har hög systemisk clearance (cirka 1,2 l/min) och halveringstiden i plasma efter intravenös dosering uppgår i medeltal till cirka 2‑3 timmar och hos barn till 1,5 timmar.
Linjäritet
Budesonids kinetik är dosproportionell vid kliniskt relevanta doser.
Pediatrisk population
Budesonid har en systemisk clearance på ungefär 0,5 liter/min hos barn med astma i åldern 4 till 6 år. Clearance per kilo kroppsvikt hos barn är ungefär 50 % högre än hos vuxna. Budesonids terminala halveringstid efter inhalation är cirka 2,3 timmar hos barn med astma. Detta är ungefär samma som hos vuxna. AUC (area under kurvan) efter administrering av 256 mikrogram budesonid från budesonid nässpray är 5,5 nmol × timmar/liter hos barn, vilket indikerar högre systemisk glukokortikosteroidexponering hos barn än hos vuxna. Vid kliniskt rekommenderade doser är farmakokinetiken för budesonid dosproportionell och plasmaexponeringen är korrelerad till patientens vikt. Detta bör därför beaktas när pediatriska doser fastställs.
Prekliniska uppgifter
Gängse studier avseende allmäntoxicitet, gentoxicitet och karcinogenicitet visade inte några särskilda risker för människa vid terapeutiska doser.
Glukokortikosteroider inklusive budesonid har framkallat teratogena effekter hos djur, inklusive gomspalt och skelettavvikelser. Liknande effekter bedöms vara osannolika för människa vid terapeutiska doser.
Innehåll
Kvalitativ och kvantitativ sammansättning
Desonix 32 mikrogram/dos nässpray, suspension
Den avgivna (uppmätta) dosen på 0,05 ml nässpray, suspension, innehåller 32 mikrogram budesonid.
Desonix 64 mikrogram/dos nässpray, suspension
Den avgivna (uppmätta) dosen på 0,05 ml nässpray, suspension, innehåller 64 mikrogram budesonid.
Hjälpämne med känd effekt:
0,06 mg kaliumsorbat per 0,05 ml nässpray, suspension
För fullständig förteckning över hjälpämnen, se avsnitt Innehåll.
Förteckning över hjälpämnen
Dispergerbar cellulosa (mikrokristallin cellulosa och natriumkarboximetylcellulosa (89:11, w/w))
Polysorbat 80
Kaliumsorbat E202
Glukos, vattenfri
Dinatriumedetat
Saltsyra, koncentrerad
Askorbinsyra E300
Vatten för injektionsvätskor
Blandbarhet
Ej relevant.
Miljöpåverkan
Miljöinformationen för budesonid är framtagen av företaget Vifor Pharma för Budenofalk, Budenofalk®, Jorveza
Miljörisk:
Användning av budesonid har bedömts medföra försumbar risk för miljöpåverkan.
Nedbrytning:
Budesonid är potentiellt persistent.
Bioackumulering:
Budesonid har låg potential att bioackumuleras.
Läs mer
Detaljerad miljöinformation
PEC/PNEC = 0.011/8.6 = 0.0013
PEC/PNEC ≤ 0.1
Environmental Risk Classification
Predicted Environmental Concentration (PEC)
PEC is based on following data and calculated using the equation outlined in the fass.se guidance (Ref 1):
PEC (µg/L) = (A*109*(100-R))/(365*P*V*D*100)
PEC (µg/L) = 1.5*10-6*A*(100-R)
A (Kg/year) = 70.1 kg total sold amount API in Sweden year 2019, data from IQVIA.
R (%) = removal rate (due to loss by adsorption to sludge particles, by volatilization,
hydrolysis or biodegradation) = 0
P = number of inhabitants in Sweden = 9 *106
V (L/day) = volume of wastewater per capita and day = 200 (default, Ref. 1)
D = factor for dilution of wastewater by surface water flow = 10 (default, Ref. 1)
(Note: The factor 109 converts the quantity used from kg to μg)
PEC = 1.5 * 10-6 * 70.1 * (100-0) = 0.011 µg/L
Metabolism and excretion
After oral inhalation budesonide undergoes an extensive degree (>90%) of biotransformation to metabolites of low corticosteroid activity on first passage through the liver. The activity of the major metabolites, 6β-hydroxy-budesonide and 16α-hydroxy-prednisolone, is less than 1% of the parent compound. The plasma elimination half-life is approximately 4 hours. No or trace amounts of unchanged drug were found in the urine after intravenous administration (Ref. 2).
Only trace amounts of budesonide are excreted unchanged in the urine of patients. As such, environmental exposure of budesonide resulting from patient use is expected to be negligible; however, the PEC does not take into consideration metabolism and therefore provides a worst-case exposure scenario.
PNEC (Predicted No Effect Concentration)
Ecotoxicity Data
|
Study Type |
Method |
Result |
Reference |
|---|---|---|---|
|
Toxicity to green algae, Pseudokirchinella subcapitata, growth inhibition test |
OECD 201 |
72 hour NOEC (growth rate) = 5.6 mg/L 72 hour LOEC (growth rate) = 8.6 mg/L 72 hour EC50 (growth rate) > 8.6 mg/L 72 hour NOEC (biomass) = 5.6 mg/L 72 hour LOEC (biomass) = 8.6 mg/L 72 hour EC50 (biomass) > 8.6 mg/L |
3 |
|
Acute toxicity to the giant water flea, Daphnia magna |
OECD 202 |
48 hour EC50 (immobility) >14 mg/L |
4 |
|
Acute toxicity to Rainbow Trout, Oncorhynchus mykiss |
OECD 203 |
96 hour LC50 (mortality) > 13 mg/L |
5 |
NOEC No Observed Effect Concentration
LOEC Lowest Observed Effect Concentration
EC50 the concentration of the test substance that results in a 50% effect
LC50 the concentration of the test substance that results in a 50% mortality
Environmental risk classification (PEC/PNEC ratio)
Short-term tests have been undertaken for species from three trophic levels, based on internationally accepted guidelines. For all three species, the EC50 values were greater than the highest test concentration and the limit of solubility of budesonide in the test medium. Therefore, to obtain a worst case PNEC value, the lowest limit of solubility of budesonide in the test media, reported for the algal study, is used. The PNEC is based on the lowest >EC50 value 8.6 mg/L (equivalent to 8600 µg/L) and an assessment factor of 1000 is applied, in accordance with ECHA guidance (Ref. 6).
PNEC = 8600 /1000 = 8.6 μg/L
Environmental risk classification (PEC/PNEC ratio)
PEC = 0.011 µg/L
PNEC = 8.6 µg/L
PEC/PNEC = 1.3 x 10-3
The PEC/PNEC ratio is < 0.1 which justifies the phrase "Use of budesonide has been considered to result in insignificant environmental risk".
In Swedish: “Användning av budesonid har bedömts medföra försumbar risk för miljöpåverkan” under the heading “Miljörisk”.
Environmental Fate Data
Budesonide is extensively metabolized (>90%), and only trace amounts of budesonide are excreted unchanged in the urine of patients. As such, environmental exposure of budesonide resulting from patient use is expected to be negligible. Budesonide cannot be considered as readily biodegradable and based on the octanol-water partition coefficient the risk of bioaccumulation in aquatic organisms is low.
Environmental Fate Data for Budesonide
|
Study Type |
Method |
Result |
Reference |
|---|---|---|---|
|
Aerobic biodegradation |
OECD301E |
Degradation after 7 days <8% Not readily biodegradable |
7 |
Degradation
Biotic degradation
Budesonide is not biologically readily biodegradable (Ref. 7). Since data from further degradation tests is lacking, the phrase ‘Budesonide is potentially persistent’ is used under the heading Biodegradation.
In Swedish: ”Läkemedlet är potentiellt persistent” under the heading ”Nedbrytning”.
Bioaccumulation
Budesonide is not ionisable within the environmentally relevant pH range. The Log octanol-water partition coefficient is 3.3, measured at pH 7.4. Since Log P < 4, budesonide has low potential to bioaccumulate and the phrase “Budesonide has low potential for bioaccumulation” is assigned.
In Swedish: Budesonid har låg potential att bioackumuleras” under the heading ’Bioackumulering’.
Physical Chemistry Data
|
Study Type |
Method |
Result |
Reference |
|
Solubility Water |
Unknown |
14 mg/L at 25 °C |
8 |
|
Octanol-Water Partition Coefficient |
Unknown |
Log Kow = 3.3 |
References
-
Fass.se (2012). Environmental classification of pharmaceuticals at www.fass.se: Guidance for pharmaceutical companies https://www.fass.se/pdf/Environmental_classification_of_pharmaceuticals-120816.pdf.pdf
-
Investigator’s Brochure. Drug Substance Budesonide/formoterol. Project Code D5890000000. Edition Number 9. Date 31 May 2016.
-
Budesonide: Toxicity to the green alga Selenastrum capricornutum. Bowles A.J. Brixham Environmental Laboratory Report BL8078/B. May 2005.
-
Budesonide: Acute toxicity to Daphnia magna. Bowles A.J. Brixham Environmental Laboratory Report BL8079/B. May 2005.
-
Budesonide: Acute toxicity to rainbow trout (Oncorhynchus mykiss). Bowles A.J. Brixham Environmental Laboratory Report BL8080/B. May 2005.
-
ECHA (European Chemicals Agency) 2008. Guidance on information requirements and chemical safety assessment. Chapter R.10: Characterisation of dose [concentration]-response for environment http://guidance.echa.europa.eu/docs/guidance_document/information_requirements_en.htm
-
Nedbrytbarhetsförhållanden för läkemedelssubstansen A002. Institutet för vatten- och luftvårdsforskning (IVL). IVL-rapport A92017. (Safety Assessment rapport SR99433-01).
-
Budesonid - preformuleringsrapport. Report no. 83 – 014. Draco, Lund, Sweden. 1 February 1983.
Hållbarhet, förvaring och hantering
Hållbarhet
18 månader
Efter första öppnandet: 3 månader
Särskilda förvaringsanvisningar
Förvaras vid högst 30 ºC
Får ej frysas.
Förvaringsanvisningar för läkemedlet efter öppnande finns i avsnitt Hållbarhet, förvaring och hantering.
Särskilda anvisningar för destruktion
Inga särskilda anvisningar.
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.
Egenskaper hos läkemedelsformen
Nässpray, suspension.
Vit till nästan vit, homogen suspension.
Förpackningsinformation
Nässpray, suspension 32 mikrog/dos
Vit till nästan vit, homogen suspension.
120 dos(er) spraybehållare, receptfri, 84:97, F, Övriga förskrivare: sjuksköterska, tandläkare
3 x 120 dos(er) spraybehållare, receptfri, 180:13, F, Övriga förskrivare: sjuksköterska, tandläkare
Nässpray, suspension 64 mikrog/dos
vit, homogen suspension
1 x 120 dos(er) spraybehållare, 188:41, F, Övriga förskrivare: sjuksköterska, tandläkare
3 x 120 dos(er) spraybehållare, 217:77, F, Övriga förskrivare: sjuksköterska, tandläkare




